青岛能源所实现手性聚酯的立体选择性解聚
手性是自然界的基本特征之一。在分子水平上,手性分子(如DNA、RNA、蛋白质)的识别和转化过程是生命活动最基本的功能,确保了高效的代谢途径、准确的遗传信息传递和正常的蛋白质功能。实现这种高选择性识别与转化的关键执行者是酶。酶通过精巧的手性活性口袋,能够精确识别底物分子的手性结构与大分子链上的特定序列,从而实现手性生物分子的构筑与转化。这种源于生命体系的手性识别能力不仅限于天然生物分子,酶对人工合成手性底物同样展现出优异的识别与催化转化能力。例如,蛋白酶Proteinase K能选择性识别聚(L-乳酸)并完成其催化水解,而聚(D-乳酸)却难以被识别,因此水解活性很低。这种强大的手性识别能力反映出酶结构设计的精巧性。
在合成化学与催化领域,通过合成催化剂(如金属配合物、有机催化剂等)实现不对称催化一直是重要的研究目标。该领域的研究曾在2001和2021年两次获得诺贝尔化学奖,突出了其重要的研究价值。然而,目前的科学研究主要集中在对手性小分子的选择性转化。相比于小分子单体,大分子具有更复杂的空间结构与手性位点排布。这一特征对合成催化剂的立体区分能力提出了更高的要求,传统的小分子催化识别机制难以适用。这一挑战使得基于合成催化剂实现对手性大分子手性识别的相关研究几乎空白。
青岛能源所催化聚合与工程研究中心致力于手性识别与催化转化的研究。在前期的研究中,实现了系列对小分子手性识别与转化的手性单体的立体选择性聚合研究(J. Am. Chem. Soc. 2024, 146, 9084−9095; Angew. Chem. Int. Ed.2025, 64, e202417075; Sci. China Chem.2025, 68, 1916–1928等)。近期,研究团队进一步拓展其研究领域,成功实现了对具有挑战性的大分子手性识别与转化。基于仿酶催化的研究思路,以具有代表性的手性聚乳酸(PLA)为模型聚合物,利用具有限域空间结构的BisSalen-Al作为催化剂,首次实现了聚乳酸的手性识别以及立体选择性解聚为手性丙交酯单体(图1)。
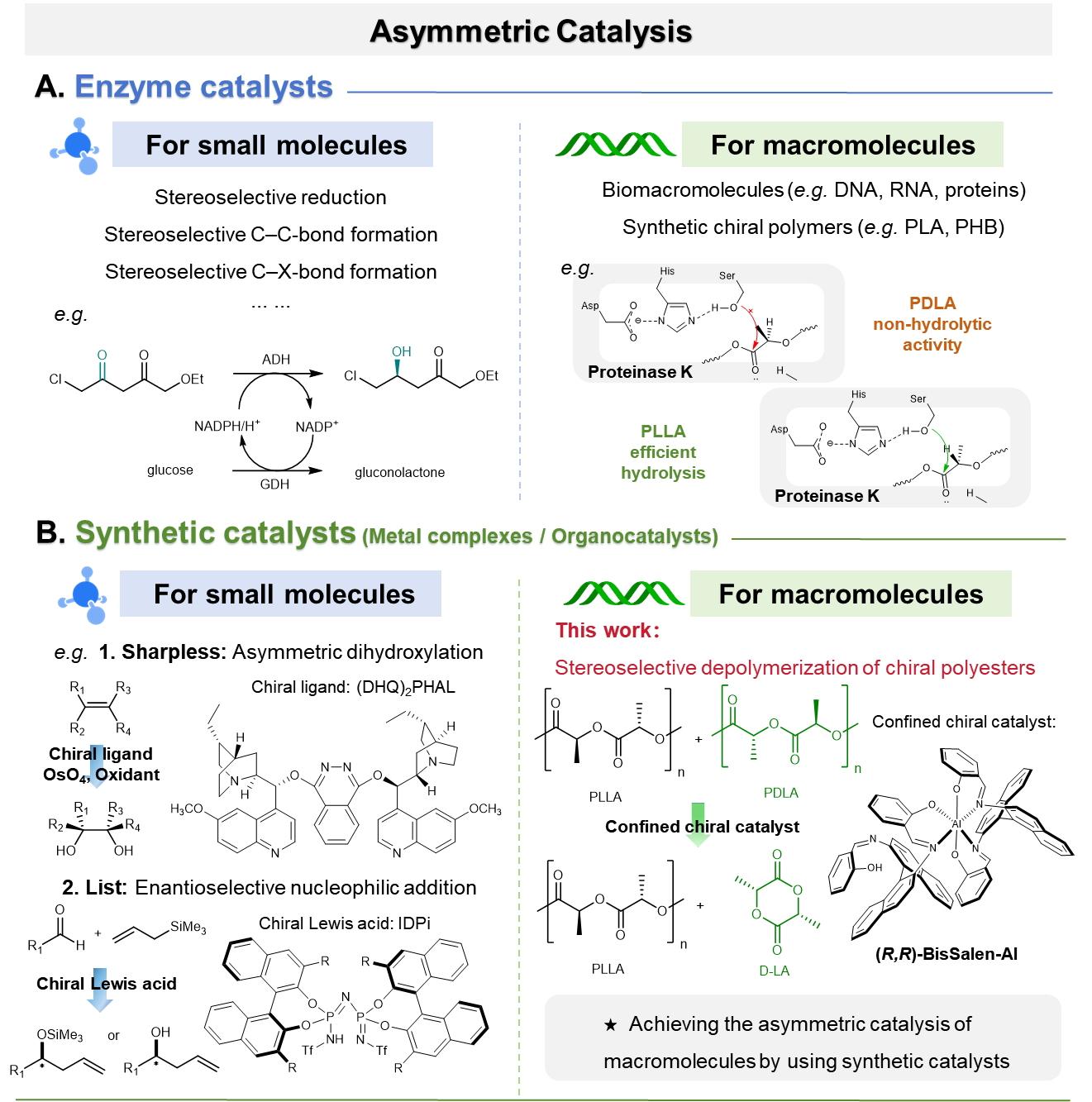
图1 利用酶和合成催化剂对小分子和大分子的不对称催化
该研究工作深入探讨了催化剂结构与解聚立体选择性之间的构效关系,揭示了催化剂的限域结构是实现对聚合物手性识别与催化转化的关键。通过优化催化剂的结构,研究人员发现两种构型聚乳酸的解聚速率差可达37.5倍,与催化剂手性匹配的聚乳酸能够高效解聚为手性单体,而不匹配的聚乳酸则难以发生解聚。为了深入理解选择性识别的机制,研究人员通过反应过程跟踪与动力学研究、催化剂结构解析、催化剂与底物作用物种分析以及DFT计算等,明确了催化剂立体选择性识别链末端并催化闭环的解聚机制。该方法进一步扩展到立构复合和手性二嵌段聚乳酸的动力学拆分解聚,获得高光学纯度的手性丙交酯单体与手性聚乳酸。该研究将不对称催化拓展到手性聚合物对映选择性转化领域。
相关研究成果近期发表于Nature Communications,并获得了审稿专家的高度认可,专家们评价该研究为“首个立体选择性解聚实例,值得在面向广泛读者的期刊中探讨”,同时也指出该研究“标志着一个引人注目的概念性进展,将不对称催化延伸至大分子领域”。催化聚合与工程研究中心杨茹琳博士为论文第一作者,徐广强研究员和王庆刚研究员为通讯作者。科研获得了中国科学院A类先导专项、国家自然科学基金、山东省自然科学基金以及山东省人才计划等项目的支持。(文/图 杨茹琳)
原文链接:https://doi.org/10.1038/s41467-026-70164-1
R. Yang, G. Xu*, X. Guo, W. Wei, Y. Jia, Q. Wang*, Stereoselective Depolymerization of Chiral Polyesters. Nat. Commun. 2026, DOI: 10.1038/s41467-026-70164-1.
附件下载: