青岛能源所与海南大学合作揭示“珊瑚-虫黄藻-共生细菌”单细胞代谢互作图谱
全球变暖背景下,珊瑚白化事件频发,珊瑚礁生态系统稳定性面临严峻挑战。气候变化引起的异常升温导致珊瑚、虫黄藻及共生微生物之“珊瑚全共生体”失衡甚至崩溃,因此,深刻理解共生成员间互作机制,对于维持营养代谢稳态、修复珊瑚生态系统、保护海洋生态多样性具有重要基础。近日,海南大学南海国重实验室与青岛能源所单细胞中心合作,通过活细胞稳定同位素标记与元拉曼组技术相结合,开发了珊瑚样品的原位代谢物检测方法,发现了“珊瑚—虫黄藻—共生细菌”之间碳、氮元素的传递与循环规律。这一珊瑚全共生体单细胞原位代谢图谱的首期版本,为共生体的理性重构与珊瑚礁的生态修复提供了实验依据与理论参考。
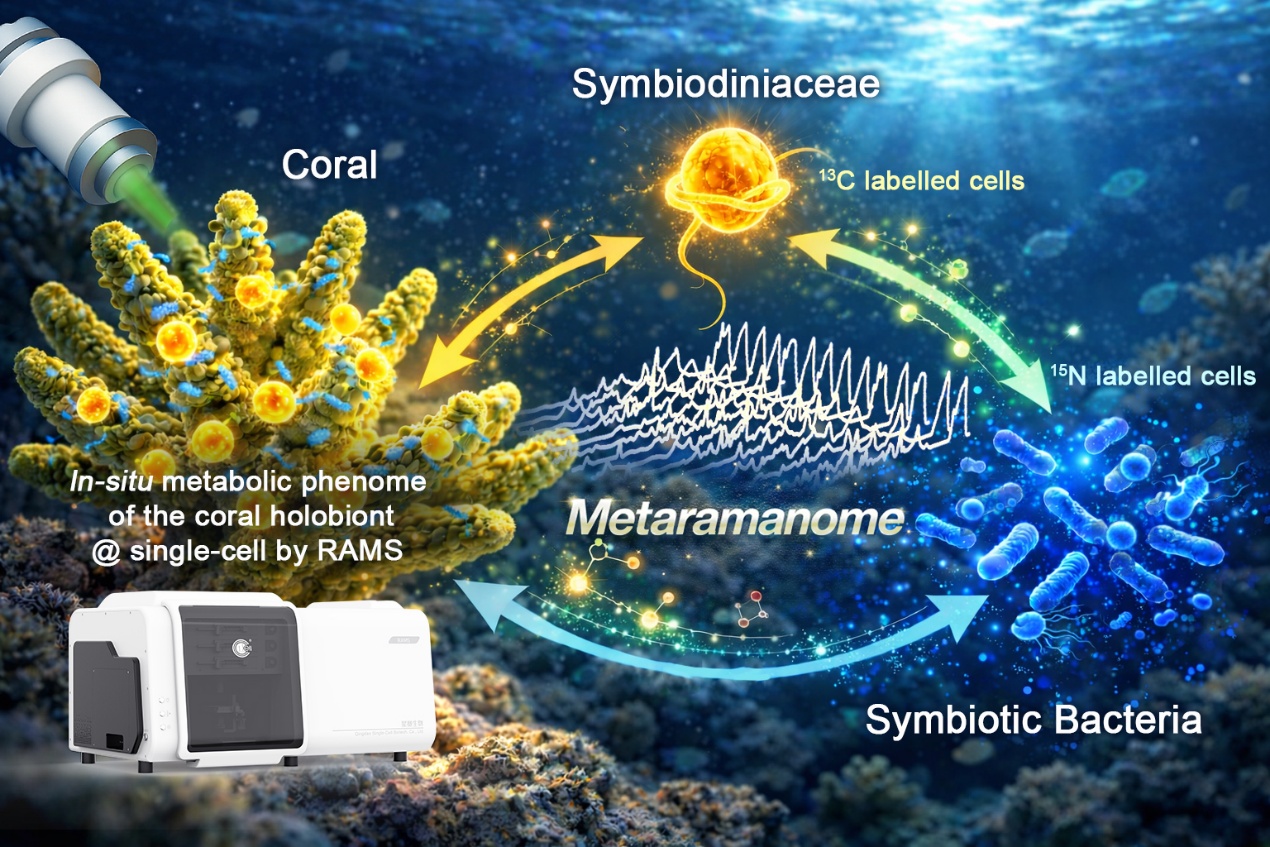
研究团队分别对珊瑚优势共生虫黄藻(C系)和一种典型的非共生虫黄藻(E系)开展了长期热驯化,在可控条件下获得了两株具有耐热表型的虫黄藻热驯化株。进而,利用青岛能源所研制的单细胞拉曼分选仪分析两株虫黄藻及其热驯化株的代谢表型,发现虫黄藻在经历热胁时,细胞内蛋白质、碳水化合物和油脂的含量明显下降,而在虫黄藻耐热株中,细胞蛋白质和油脂含量明显升高,表明代谢表型筛选可以作为定向驯化的筛选依据。同时,驯化过程中观察到部分虫黄藻细胞具有“高淀粉积累”特征,为后续突变筛选与关键性状追踪提供了潜在靶点。
结合宏基因组测序和体外实验验证,筛选到了与宿主和虫黄藻都具有密切共生关系的细菌——鼠尾菌。对两种虫黄藻热驯化株与共生菌分别进行13C 和15N 底物标记,基于底物饲喂前后单细胞拉曼光谱的比较,解析了共生细菌与两株虫黄藻之间的碳、氮元素循环。结果显示,共生细菌与不同虫黄藻之间的物质传递效率与代谢物交换特征存在差异。在共生细菌和E系虫黄藻的互作组合中,二者间交换的代谢物以氨基酸类物质为主。相比之下,共生细菌与C系虫黄藻之间的物质交换效率更高,二者不仅发生氨基酸和碳水化合物的交换,还存在核酸类化合物的双向转移。这提示说明细胞间代谢物交换的方向性及其发生的时间顺序可能是影响共生代谢效率的重要因素。
为阐明虫黄藻、共生细菌与珊瑚之间的营养互作模式,本研究针对珊瑚这一复杂生物样品,率先建立了基于单细胞拉曼光谱的原位代谢物检测流程(图1),用于跟踪珊瑚生化组成变化与白化进程之间的关系,即随着白化进程的加重,珊瑚组织会丢失大量蛋白质、脂质和碳水化合物,如若不加以干涉,珊瑚会因能量匮乏而逐渐死亡。在此基础上,提出“微生物辅助的全共生体重构”方法学框架(图1):向白化的风信子鹿角珊瑚分别加入13C标记的两种虫黄藻热驯化株与15N标记的共生细菌,在实验室水平上完成珊瑚共生体的重构,观察珊瑚的白化恢复并利用元拉曼组手段检测其代谢表型。
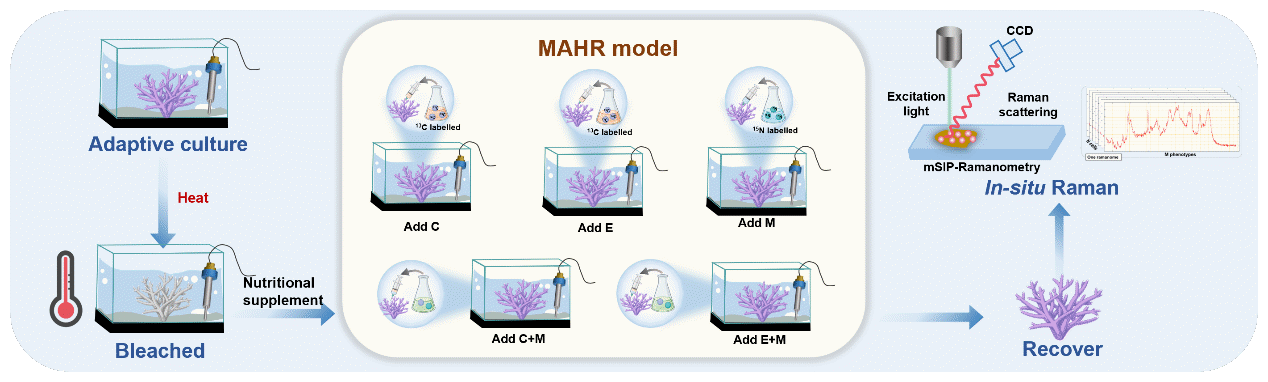
图1 元拉曼组手段检测珊瑚的代谢表型
研究发现,尽管短期内在各组珊瑚的白化恢复表型上未观察到显著差异,但引入的两种热驯化虫黄藻株及其共生细菌均能对珊瑚组织的生化组成有调控作用(图2)。在接种C系驯化株与共生细菌的处理组中,珊瑚组织内蛋白质、脂质及碳水化合物的含量均有不同程度上升,表明珊瑚的生理损伤可能得到缓解;同时,与单独处理相比,二者联合处理的效应更为明显。值得注意的是,引入E系驯化株后,珊瑚组织中出现了碳水化合物信号的积累,提示二者间存在短暂摄食关系。进一步的显微观察与核酸定量分析结果证实,E系驯化株在短期内可与珊瑚建立共生关系,并影响了珊瑚的营养分配与代谢状态。上述结果提示,在高温胁迫后珊瑚重新招募共生藻的过程中,非典型共生藻类亦可能通过共生重构获得定植机会。
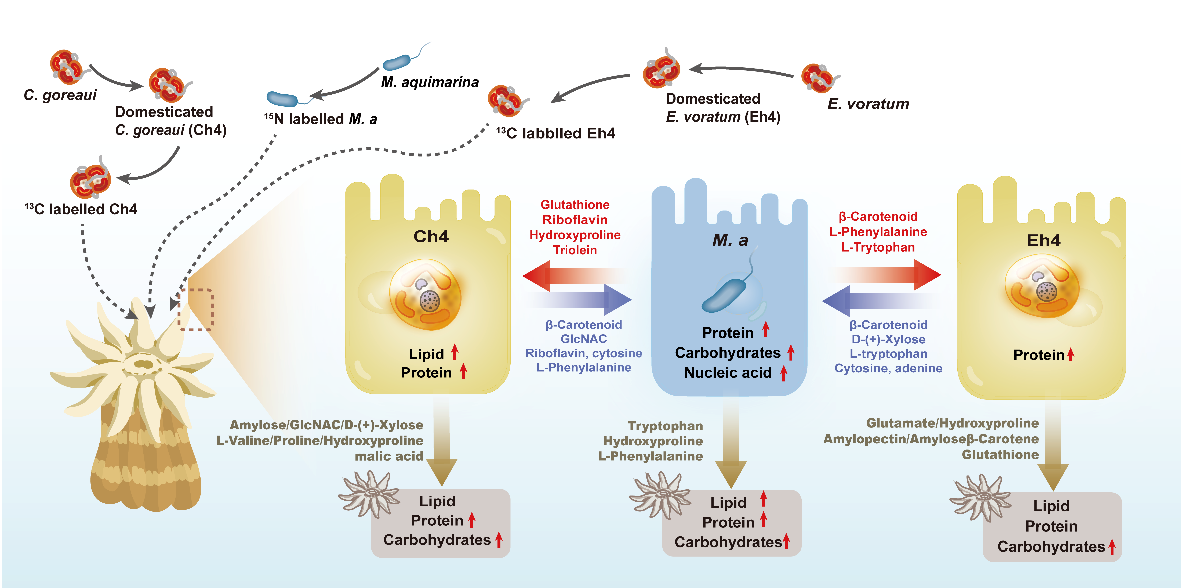
图2 用元拉曼组手段解析单细胞精度的珊瑚-虫黄藻-共生细菌间碳元素、氮元素代谢互作图谱
本研究基于耦合稳定同位素饲喂的元拉曼组手段,描绘了“珊瑚—虫黄藻—共生细菌”之间的碳、氮元素传递与循环图谱。这些发现加深了对复杂生态系统中跨界代谢与营养互作的理解,也为评估和挖掘有益微生物来缓解热胁迫下珊瑚白化风险,提供了理论基础。同时,这一活体单细胞代谢互作解析方法学体系对于单细胞原位代谢图谱(iMAPS)科学计划中其他共生体研究也具共性支撑作用。
相关成果发表于国际期刊 Microbiome。论文的第一作者为海南大学博士研究生舒杨,由海南大学南海国重实验室傅鹏程教授和青岛能源所单细胞中心徐健研究员合作主持完成,得到了海南大学科研启动资金、国家重点研发项目、国家自然科学基金等项目的大力支持。(文/舒杨 图/刘阳、舒杨)
原文链接:https://doi.org/10.1186/s40168-026-02338-4
Yang Shu, Yuehui He, Tianhui Chen, Yuanyuan Zhou, Yawen Liu, Pengcheng Fu*, Jian Xu*. Reconstruction of coral holobionts and elucidation of the causal relationships among symbiodiniaceae, bacteria, and coral through single-cell Raman spectroscopy metabolomics. Microbiome, 2026.
附件下载: