青岛能源所嗜热微生物β-木糖苷酶功能机制研究取得进展
近日,青岛能源所一碳生物技术研究中心在极端嗜热微生物糖苷水解酶功能解析与工业应用研究领域取得新进展。研究团队从极端嗜热厌氧菌解糖热解纤维素菌(C. saccharolyticus)中,成功鉴定出两个全新的GH39家族β-木糖苷酶CsXyl39A与CsXyl39B,并完成了系统的酶学性质表征与功能机制解析。这两个酶均展现出优异的嗜热特性,最适反应温度分别达75 ℃和80 ℃,同时具备金属离子非依赖性和非离子型表面活性剂高耐受性等优势,适配应用于工业复杂反应环境。
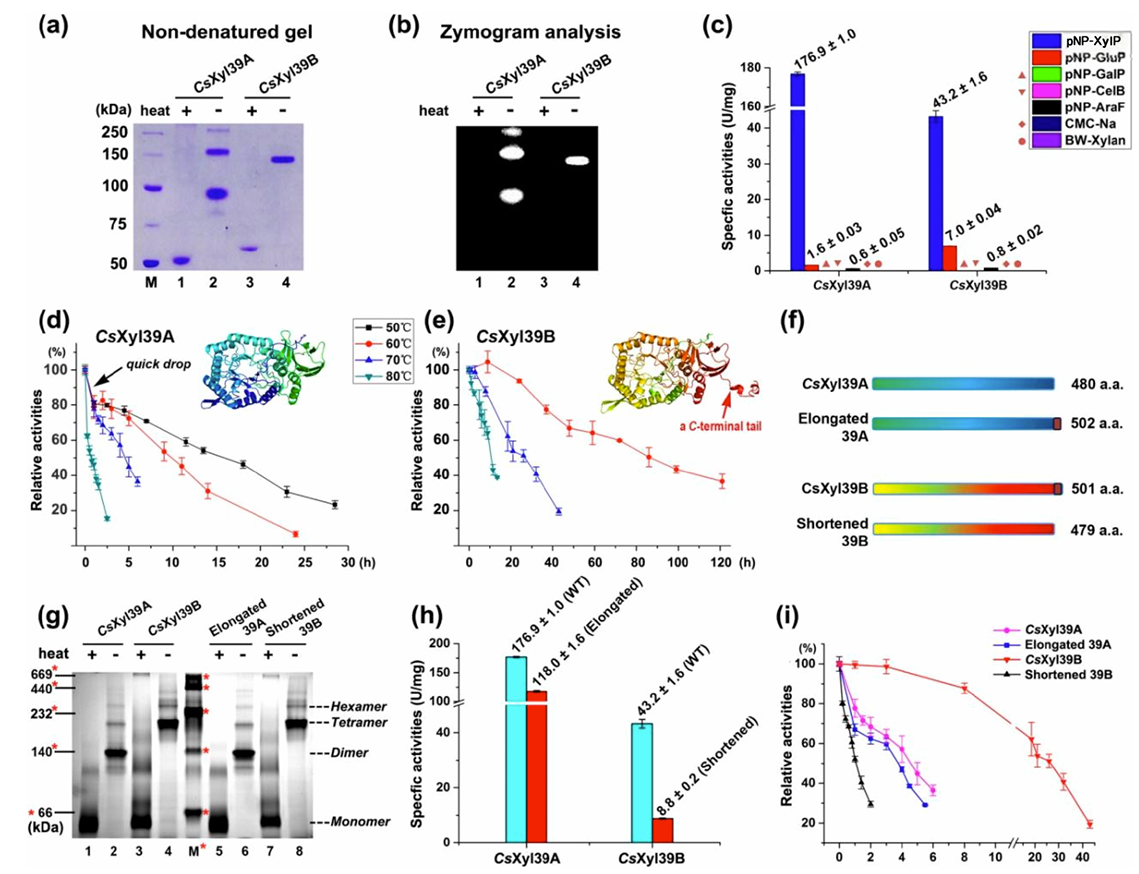
研究表明,CsXyl39B的热稳定性与产物抗逆性突出,其在70 ℃半衰期长达26小时,且在300 mM高浓度木糖中仍保留89.6%的酶活,彻底解决了传统β-木糖苷酶面临的终产物抑制瓶颈。此外,该酶与内切木聚糖酶协同作用时,可使木聚糖糖化效率提升16.7%-31.9%,是木质纤维素生物质高温糖化工艺的理想酶元件。另一方面,酶CsXyl39A展现出罕见的有机溶剂耐受性,在水/有机溶剂混溶体系中,其催化效率与热稳定性显著提升,可特异性水解三七皂苷R1的D-吡喃木糖基团,定向生成高附加值的人参皂苷Rg1。研究团队进一步通过固定化技术,大幅提升了该酶在高比例有机溶剂体系中的催化性能,60%丙酮体系中酶活仍保持112.2%,性能优于已报道的同类酶。
在此基础上,团队通过结构预测与定点突变,首次揭示了C端α-螺旋短尾(sHT)是调控GH39家族β-木糖苷酶四聚体稳定性与热稳定性的关键结构元件,这一发现为糖苷水解酶的蛋白质工程改造、热稳定性定向提升提供了全新的靶点与理论依据。
该研究不仅挖掘到两个性能互补、工业应用潜力突出的新型β-木糖苷酶,还深入阐明了GH39家族酶蛋白的热稳定性调控机制,为极端嗜热微生物糖苷酶资源的开发利用奠定了重要的理论与技术基础。
相关成果以Characterization and Functional Mechanism Analysis of Two Glycoside Hydrolase Family-39 β Xylosidases Identified from Caldicellulosiruptor saccharolyticus为题,发表于农林科学领域期刊Journal of Agricultural and Food Chemistry。论文第一作者为苏航和韩文杰,通讯作者为张慧丹副研究员与吕明研究员。本研究得到了国家重点研发计划、山东省重点研发计划、山东省博士后创新项目和青岛市博士后项目等资助。(文/图 苏航、张慧丹)
原文链接:https://doi.org/10.1021/acs.jafc.5c06093
Su H#, Han W#, Hamouda H I, Zhang H*, LU M*. Characterization and Functional Mechanism Analysis of Two Glycoside Hydrolase Family-39 β-Xylosidases Identified from Caldicellulosiruptor saccharolyticus. J. Agric. Food Chem. 2026.
附件下载: